
質量パーセント濃度の計算問題集 基本編 Menon Network
比熱と熱容量の求め方 もう一度,比熱と熱容量の違いも兼ねて,その求め方について説明します。 これらの違いは,比熱が 1 g 1\mathrm{g} 1 g あたりの温度変化に必要な熱量であった質量/体積(容積)パーセント濃度の求め方 溶質の質量 (g) ÷ 溶液の体積・容積 (ml) × 100 = 質量/体積パーセント濃度 % 体積(容積)ml にしめる、溶質の割合を求める方法です。 質量パーセント
溶液 の 質量 の 求め 方
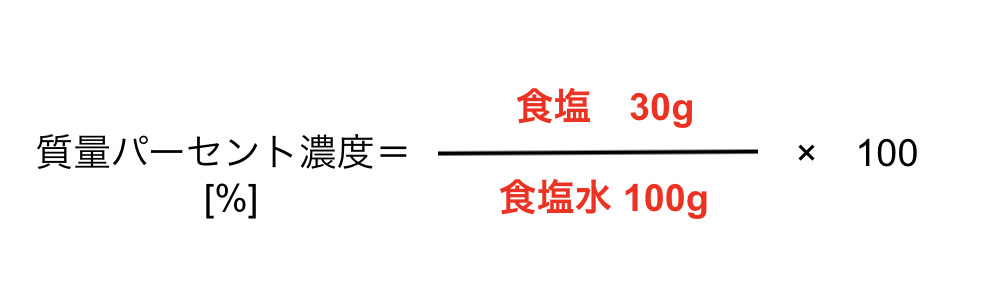
溶液 の 質量 の 求め 方- 濃度(%)=溶質の重さ(g)÷水溶液の重さ(g)×100 この値を質量パーセント濃度ともいいます。 単に濃さという場合は、この質量パーセント濃度を指します。 パーセントという溶液の濃度 「化学基礎」では、自分たちの身の回りの物質や現象などに興味を持って、鈴木福さんと一緒に考察していきましょう! 福 「海の
中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu
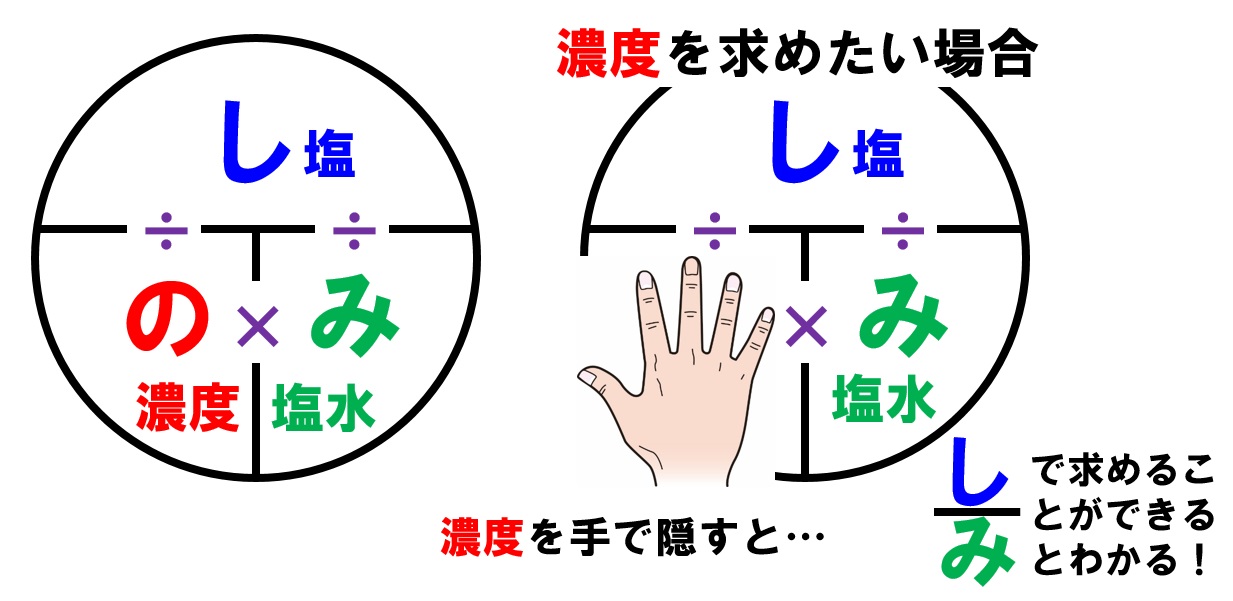
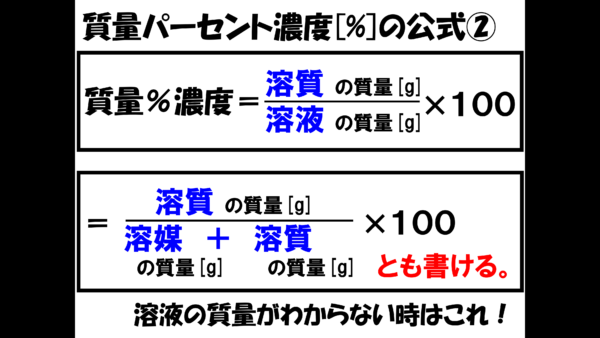
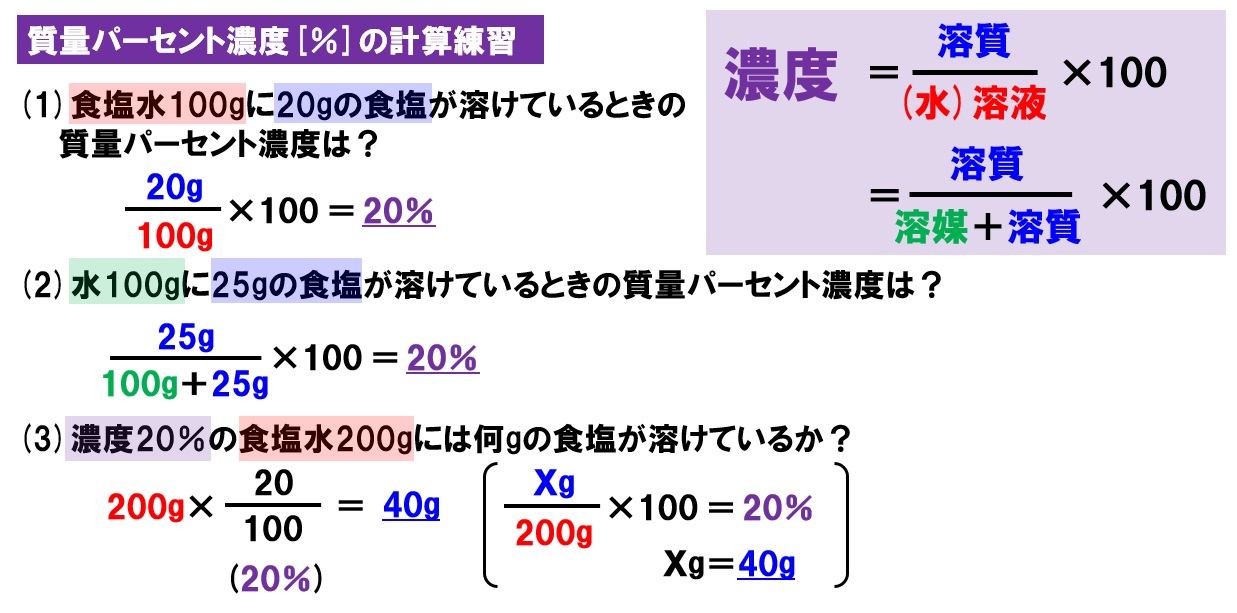
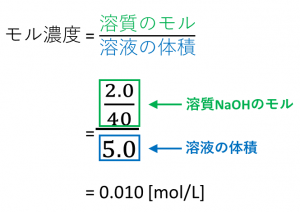
質量パーセント濃度=溶質÷溶液×100 となります! 後ろに100を掛けているのは、出てきた値を百分率で表したいからです。 なので、出てきた値に必ず%をつけましょう! また、溶液は溶質と溶ホーム » 理科 » 化学 » 濃度の計算が苦手な人必見! 公式と練習問題を元製薬会社研究員がわかりやすく解説 問題1 質量パーセント濃度15%の水酸化ナトリウム(NaOH)溶液の密度は10g /cm3 「溶媒の密度が1006g/ml、質量が490mg」→490 mg/ (1006×10^3 mg/mL)=0487 mL=487 uL で、 体積比=/ ()=16×10^ (2) と小さく、 精度も3桁は必要な
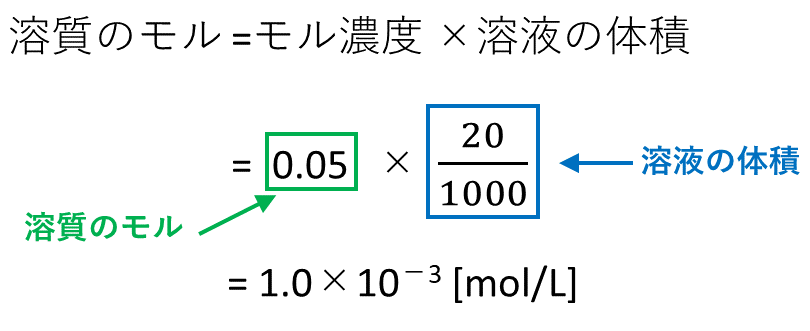
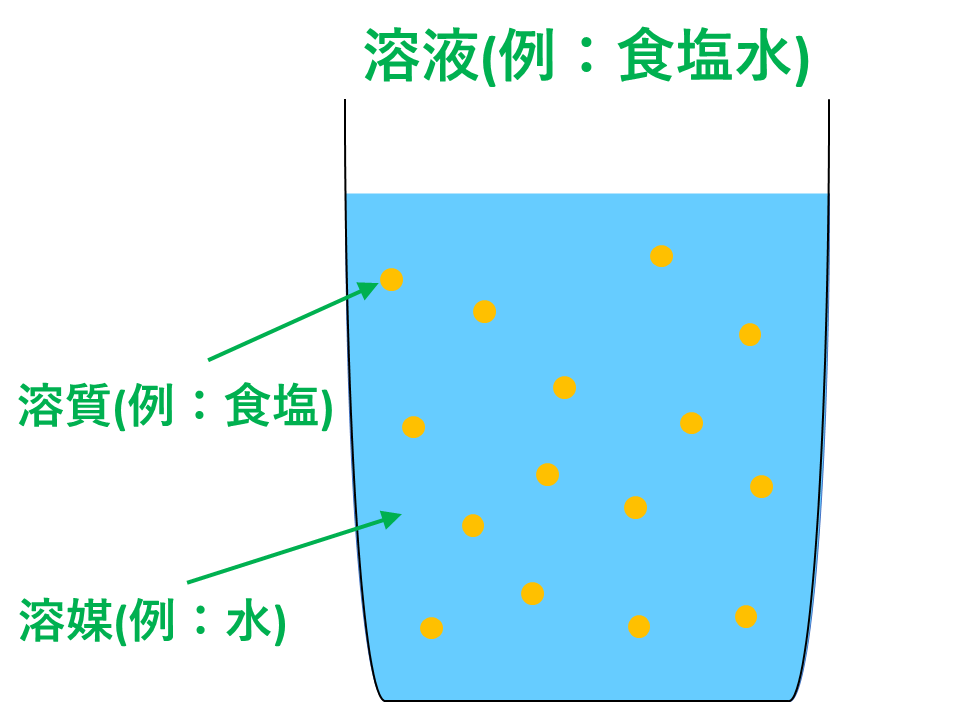
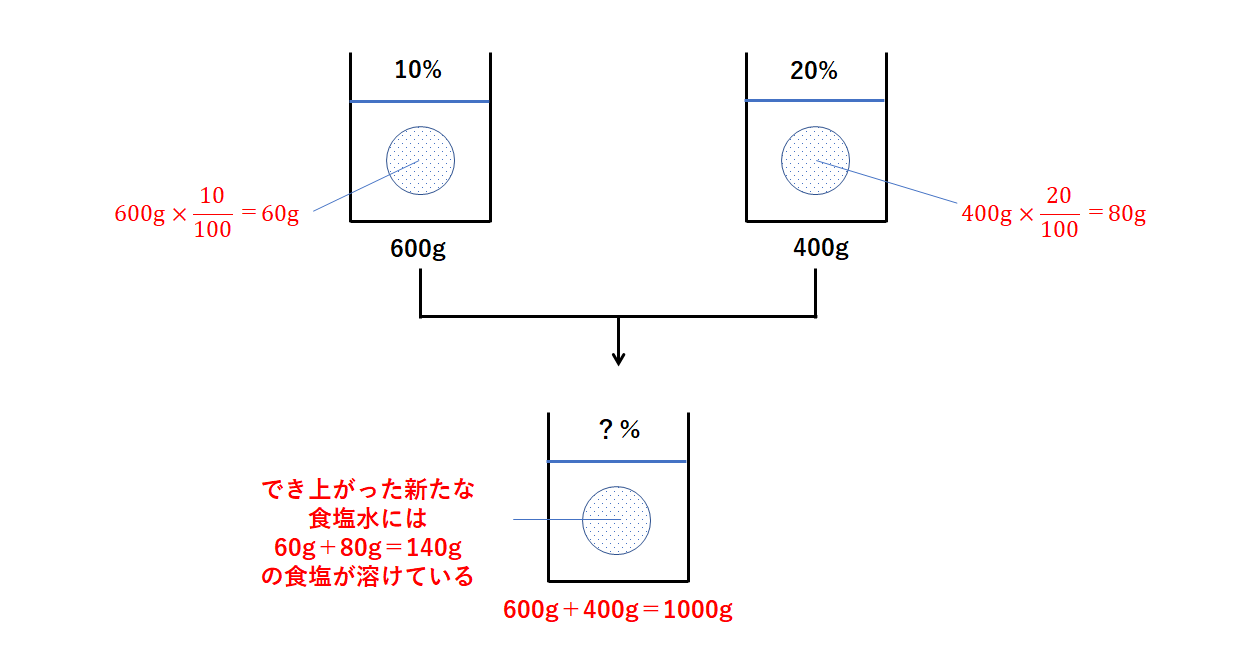
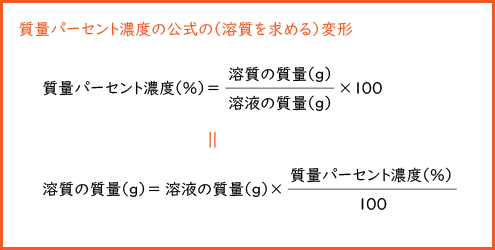
11「溶質」「溶媒」「溶液」について理解しよう 12濃度が違うとはどういうことか? 2濃度の単位と求め方 21質量百分率濃度(%) 22モル濃度( mol / L ) 23質量パーセント濃度とモル溶液の質量は、溶質の質量 + 溶媒の質量 溶質の質量は、溶液の質量×質量パーセント濃度÷100 溶媒の質量=溶液の質量×(溶液の質量-質量パーセント濃度÷100)溶液の濃度とその表し方 1原子量と分子量 定義・説明 原子量は質量数12の炭素同位体( )の質量を12とした時の、他の元素の相対的質量である。 したがって、原子量は無次元で単位はない。 分子
溶液 の 質量 の 求め 方のギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic | 質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic | 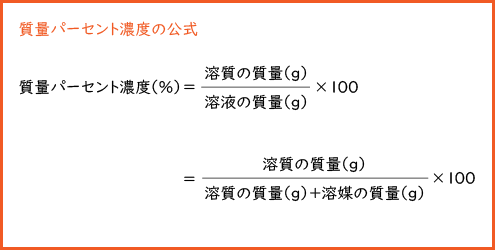 質量モル濃度 Okedic |
 質量モル濃度 Okedic | 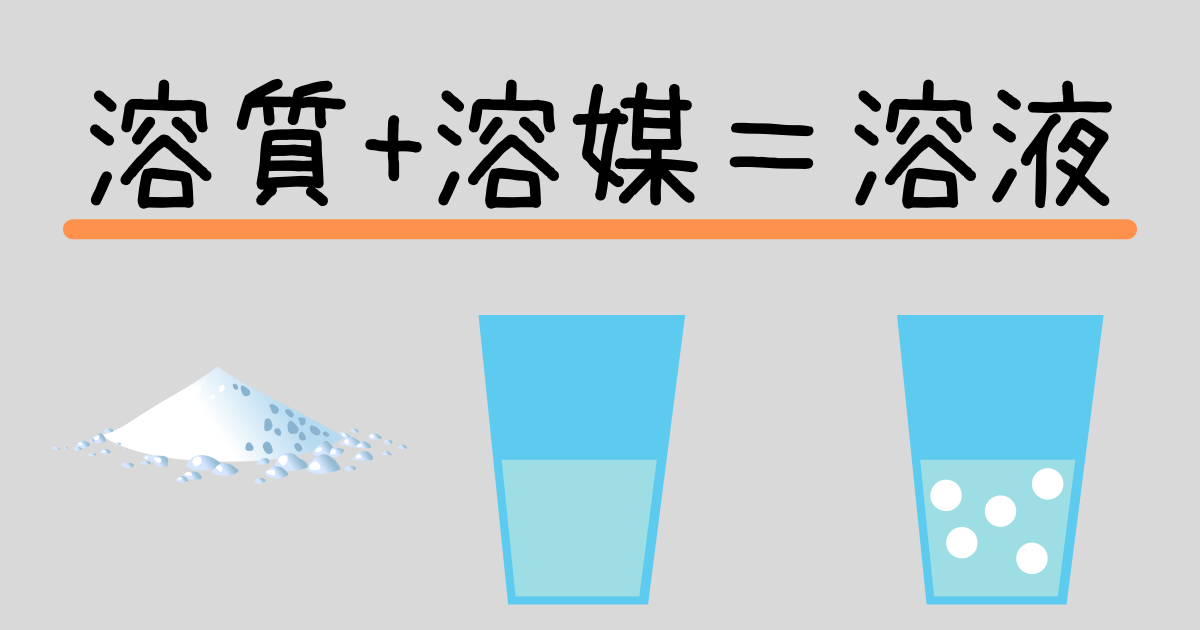 質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic | 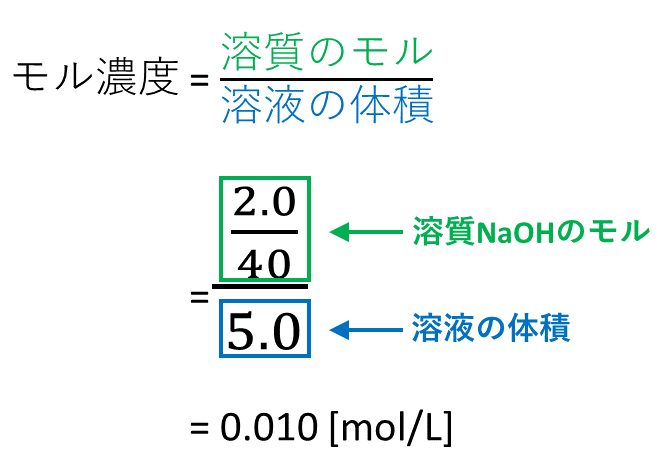 質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic | 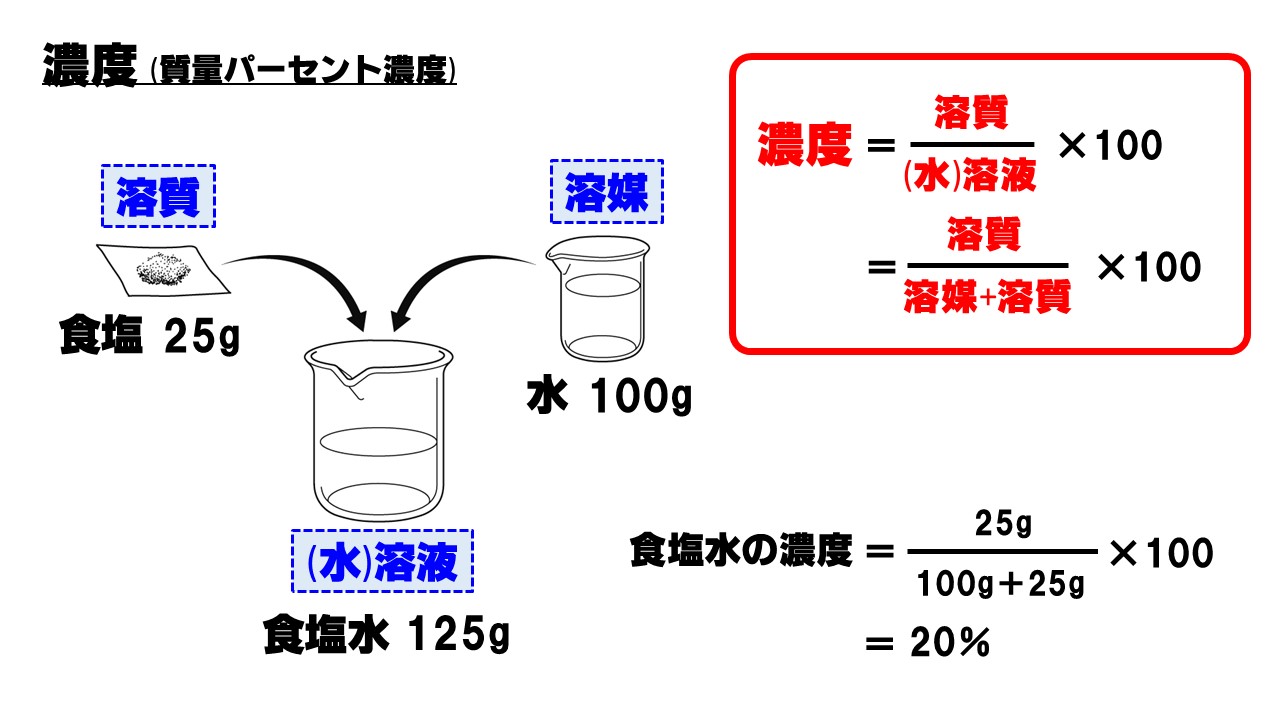 質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic | 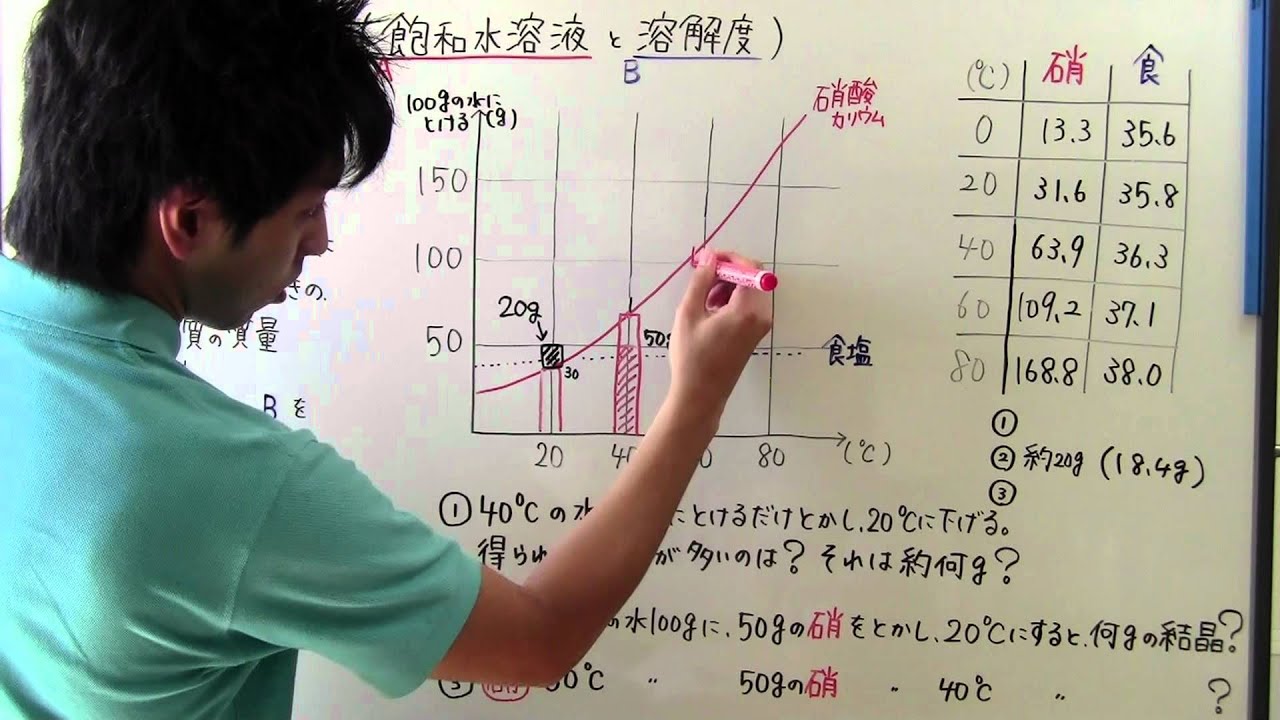 質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic | 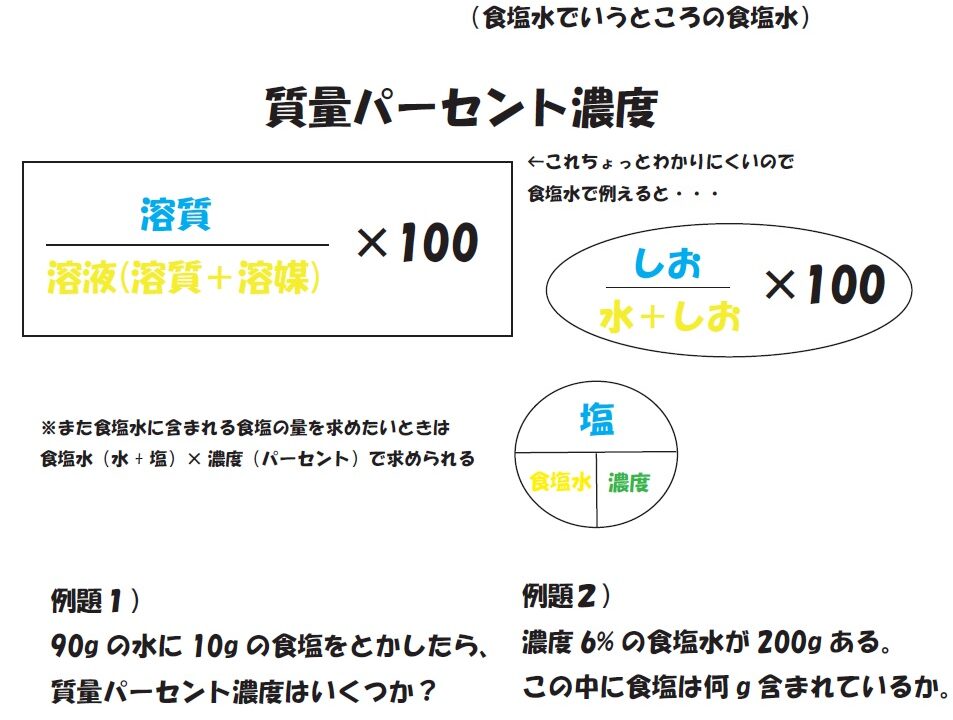 質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic | 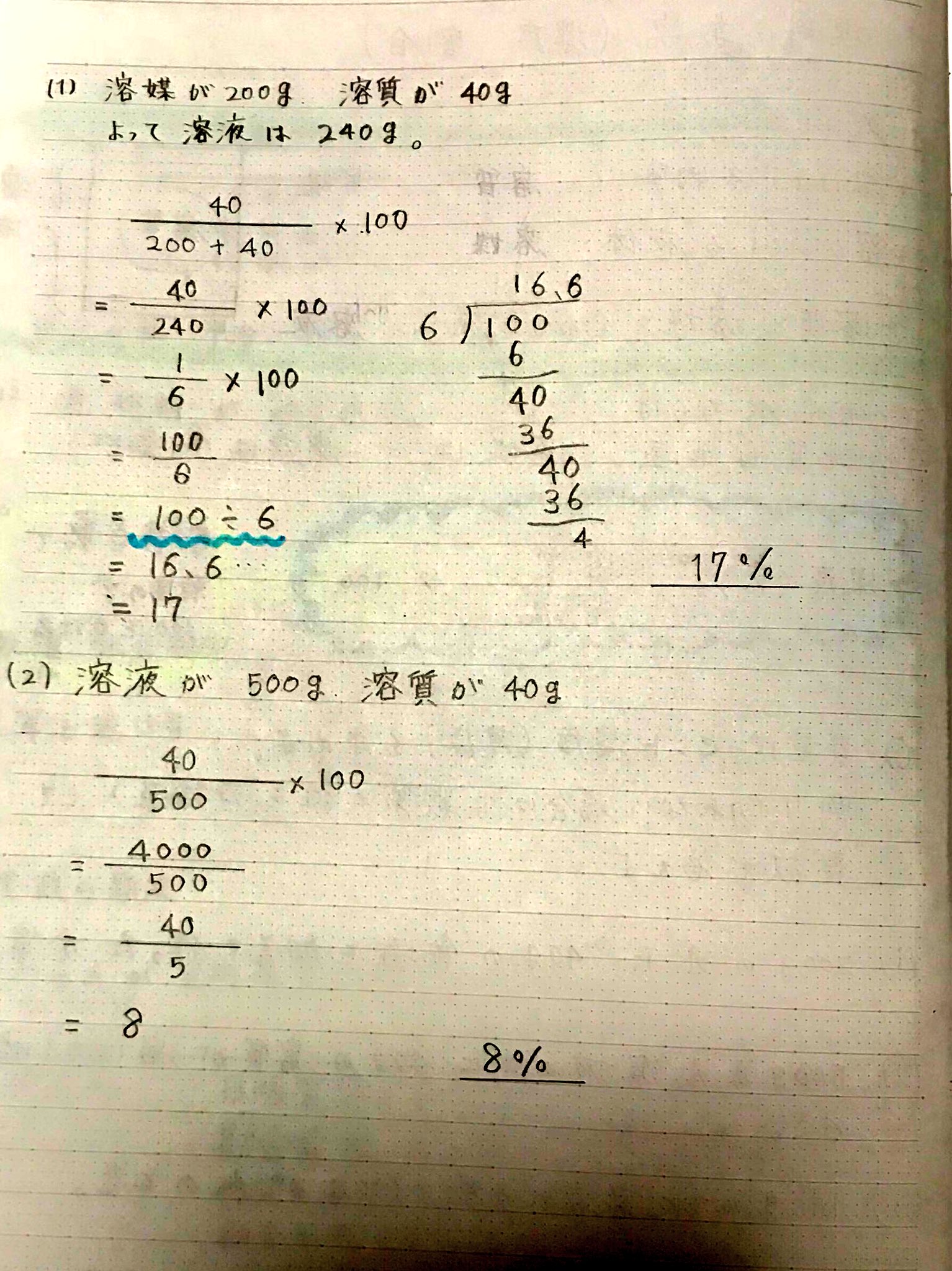 質量モル濃度 Okedic | 質量モル濃度 Okedic |
 質量モル濃度 Okedic | 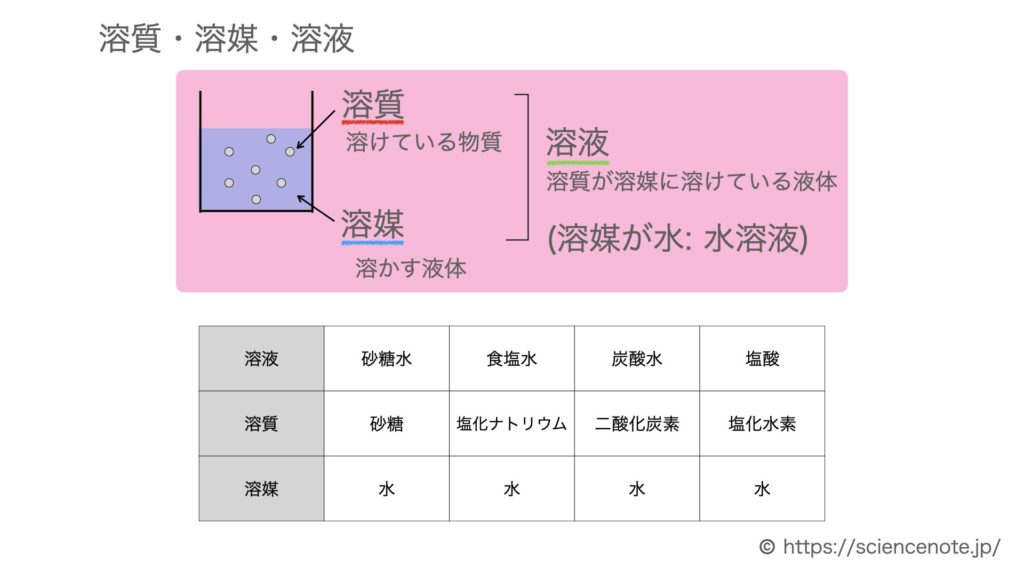 質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic | 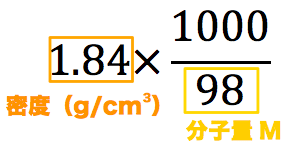 質量モル濃度 Okedic | 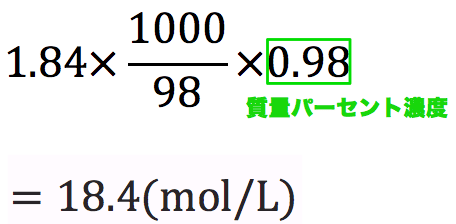 質量モル濃度 Okedic |
質量モル濃度 Okedic | 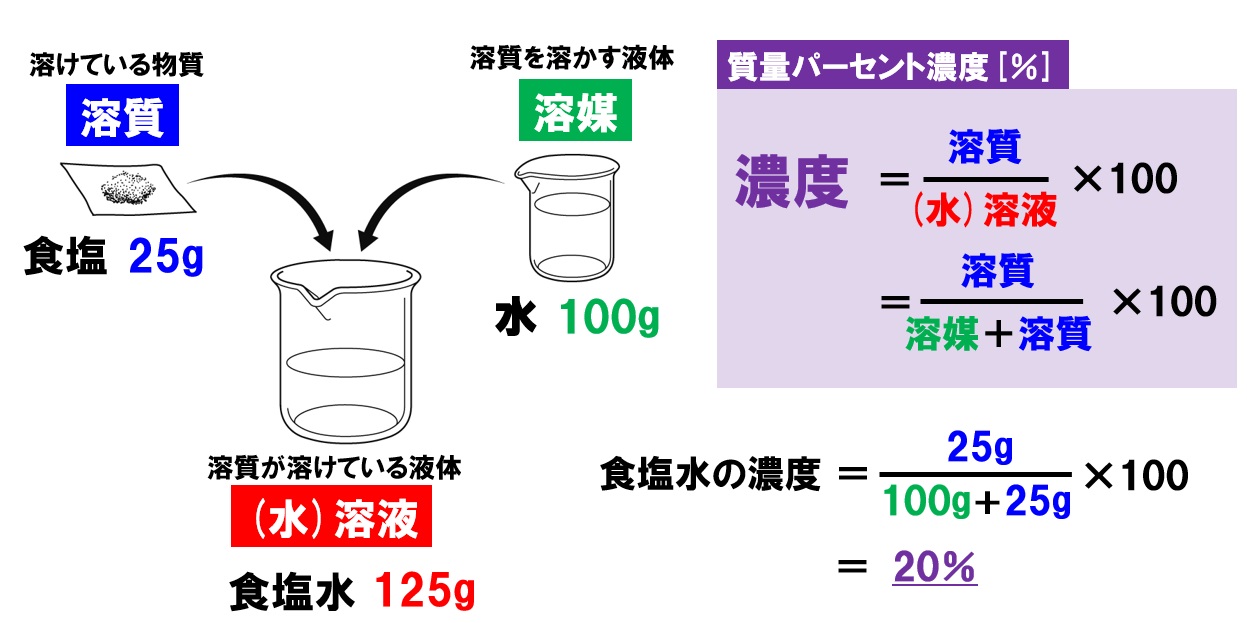 質量モル濃度 Okedic | 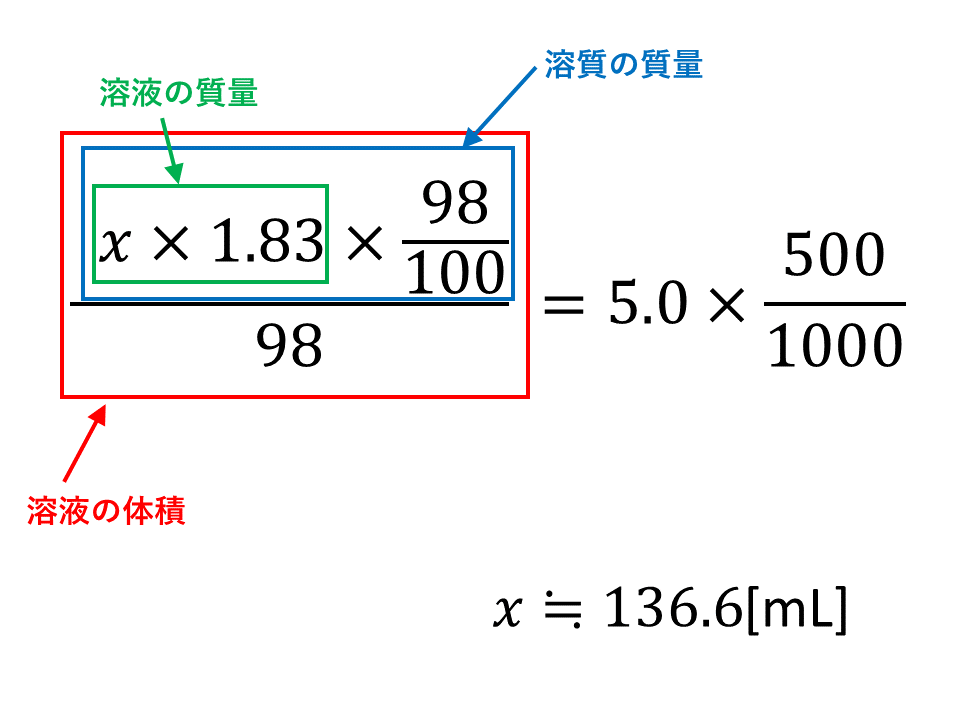 質量モル濃度 Okedic |
 質量モル濃度 Okedic | 質量モル濃度 Okedic | 質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic | 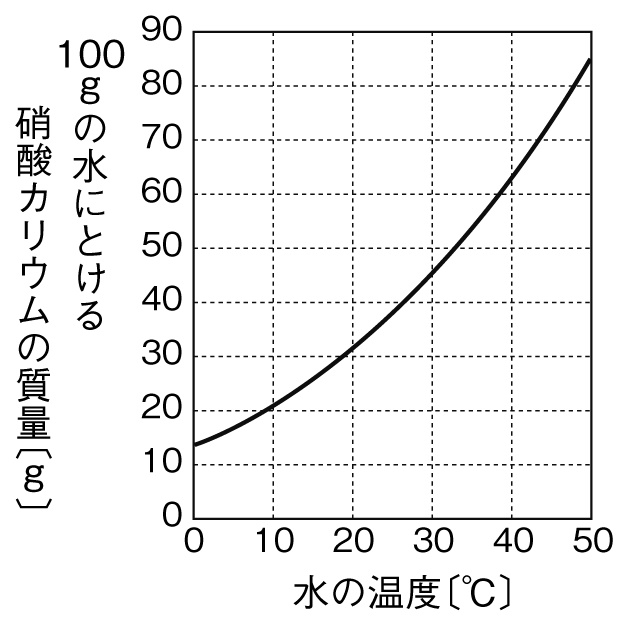 質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic | 質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
質量モル濃度 Okedic |  質量モル濃度 Okedic | 質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic | 質量モル濃度 Okedic |
 質量モル濃度 Okedic |  質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic | 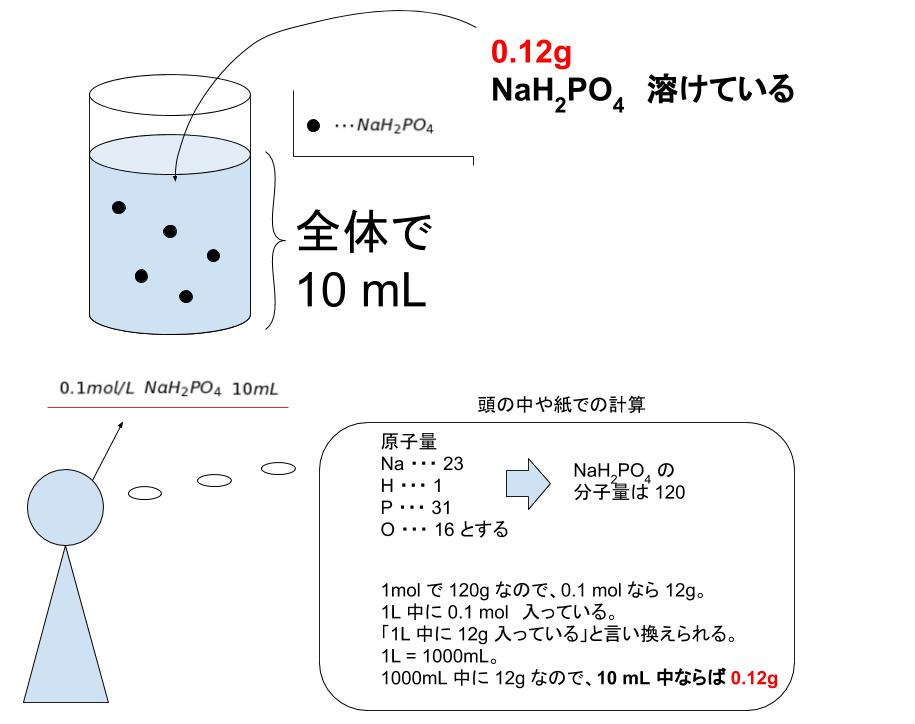 質量モル濃度 Okedic |  質量モル濃度 Okedic |
 質量モル濃度 Okedic | 質量モル濃度 Okedic |
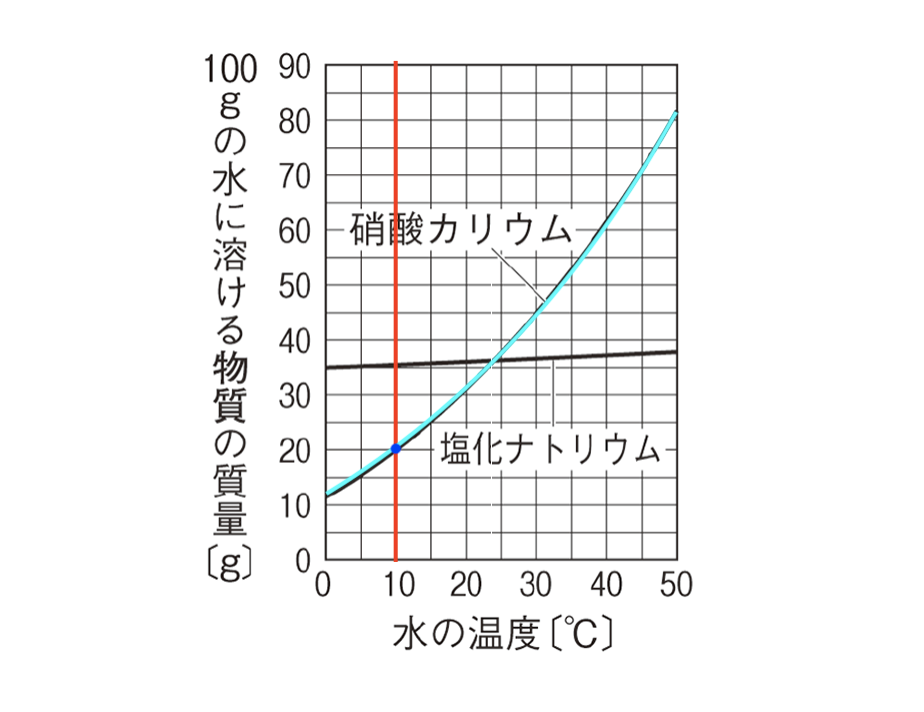
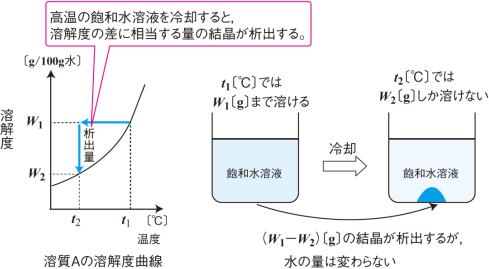
2 水を蒸発させる問題を解いていく 21 ステップ1:変化後の温度と溶解度を確認;今回は、反応速度式を使って溶解平衡の成立している溶液中のイオン濃度について考えます。 溶解速度や析出速度は素反応の反応速度式と同じように表せます。 この溶解平衡は AgCl (固) ↔ AgCl




